- ОРДИ
- Каналы
- Риносинусит как междисциплинарная проблема
- Систематический обзор: лечение острого риносинусита растительными препаратами с точки зрения доказательной медицины.
Основные положения
- Рекомендации консервативной терапии ОРС по рекомендациям EPOS-2020 и ICAR: Rhinosinusitis (RS)
- Алгоритм ведения пациентов по EPOS-2020
- Оценка доказательной базы препаратов, применяемых в консервативной терапии ОРС
- Выводы проведенного анализа качества исследований
- Анализ доказательной базы
- 5.1 ⠀Синупрет®
- 5.2 ⠀Экстракт пелларгонии сидовидной (Pelargonium sidoides)
- 5.3 ⠀Цикламен (Cyclamen europaeum)
- 5.4 ⠀ГелоМиртол® форте
- 5.5 ⠀Цинеол
- 5.6 ⠀Мометазона фуроат
- 5.7⠀ N-ацетилцистеин
- Приложение
Рекомендации консервативной терапии ОРС по рекомендациям EPOS-2020 и ICAR: Rhinosinusitis (RS)
Острый риносинусит (ОРС), распространенная инфекция верхних дыхательных путей, оказывает существенное влияние на качество жизни и приводит к высоким социально-экономическим издержкам [1, 2].
· Европейский согласительный документ по риносинуситу и назальным полипам (European position paper on rhinosinusitis and nasal polyps – EPOS) от 2020 г. рекомендует использовать антибиотики только при риносинусите бактериального происхождения [1].
· А Международный консенсус по аллергии и ринологии: риносинусит (International Consensus Statement on Allergy and Rhinology: Rhinosinusitis (ICAR: RS) рекомендует использовать консервативный подход к применению антибиотиков на том основании, что ОРС даже бактериального происхождения имеет высокую вероятность самопроизвольного разрешения [3].
В случае вирусного ОРС (банальной простуды) у взрослых и детей рекомендации EPOS с высоким уровнем доказательности 1а и 1b поддерживают использование:
· антигистаминных препаратов
· деконгестантов (в т.ч. пероральных)
· ацетаминофена (парацетамол)
· нестероидных противовоспалительных средств
· комплексных средств от простуды
· ипратропия бромида
· орошения полости носа солевым раствором
· растительных лекарственных препаратов, за исключением эхинацеи (Синупрет экстракт - BNO1016, экстракт цинеола и андрографиса метельчатого SHA-10)
· пробиотиков, витамина С, физических упражнений, препаратов цинка и фюзафюнжина (препарат выведен с рынка в 2016 году в связи с развитием серьезных аллергических реакций, включая бронхо- и ларингоспазм)
При этом применения антибиотиков рекомендуется избегать.
Алгоритм ведения пациентов по EPOS 2020
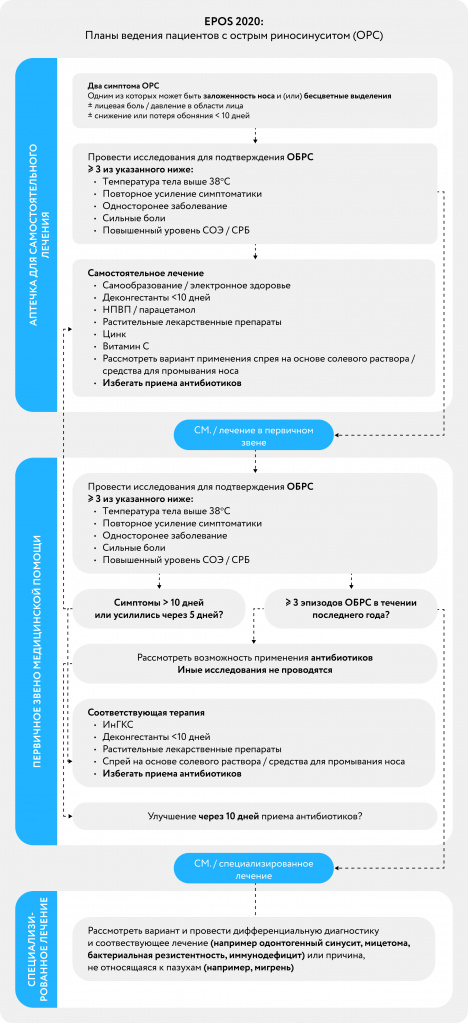

Оценка доказательной базы препаратов, применяемых в консервативной терапии ОРС
Несмотря на существование указанных рекомендаций по применению антибиотиков, в лечении ОРС их продолжают достаточно часто использовать, что способствует распространению устойчивых к антибиотикам штаммов бактерий по всему миру [4].
Одним из вариантов решения проблемы чрезмерного использования антибиотиков в этой ситуации является поиск альтернативных методов лечения РС, позволяющих как вылечить инфекцию, так и контролировать симптомы. Такими средствами являются растительные лекарственные препараты, доказавшие свою эффективность в рандомизированных клинических, в том числе слепых плацебо-контролируемых, исследованиях [5-8].
Клинические исследования растительных препаратов, используемых для консервативной терапии риносинусита, разнятся как по количеству, так и по качеству доказательности.
Для оценки доказательной базы эффективности и безопасности лечения ОРС с помощью растительных препаратов в январе 2019 г. в базе данных MEDLINE был произведен поиск клинических исследований, из которых, согласно критериям качества, были отобраны исследования 5 растительных лекарственных препаратов:
1. Синупрет®
2. Экстракт Pelargonium sidoides
3. Cyclamen europaeum (цикламен)
4. Цинеол
5. ГелоМиртол® форте
В ходе анализа данных провели оценку доказательной базы отобранных растительных препаратов, а также двух синтетических препаратов:
6. N-ацетилцистеина
7. Мометазона фуроата (МФ).
Выводы проведенного анализа доказательности исследований
Была проведена оценка ряда растительных препаратов для лечения ОРС в рандомизированных клинических исследованиях:
· для препаратов, произведенных согласно концепции Фитониринг®, Синупрет® и Синупрет®экстракт, представлена самая сильная доказательная база, включая многоцентровые клинические исследования с большим уровнем достоверности,
· за ним следует экстракт Pelargonium sidoides (EPs 7630), эффективность которого подтверждают небольшие исследования,
· из всего ряда других растительных препаратов, включая назальный спрей цикламена, ГелоМиртол® и цинеол, для каждого препарата доступно в лучшем случае только одно рандомизированное исследование,
· среди синтетических методов лечения, описанных в настоящем обзоре, для назального спрея МФ представлены самые убедительные доказательства,
· интересно, что доказательства для Синупрета® столь же сильны, что и для синтетических препаратов, таких как назальный спрей МФ.
Синупрет® экстракт (BNO 1016) – единственный растительный препарат, в отношении которого имеются данные, полученные в результате должным образом разработанных и проведенных клинических исследований с достаточной мощностью.
В контексте растущей резистентности микроорганизмов и нерационального применения антибиотиков выбранные растительные препараты являются многообещающей альтернативой традиционным методам лечения острого неосложненного РС.
Анализ доказательной базы растительных препаратов
Синупрет
О препарате:
Синупрет® применяется для лечения синусита с 1934 г. [9].
Это растительный препарат, содержащий смесь:
· Gentianae radix,
· Primulae flos cum calycibus,
· Sambuci flos,
· Rumicis herba
· Verbenae herba [10].
Доклинические исследования показывают, что Синупрет® оказывает благоприятное воздействие на ОРС благодаря своим свойствам:
· секретолитическим
· муколитическим,
· противовоспалительным
· противовирусным,
· умеренным антибактериальным [11, инструкция по мед применению].
Синупрет® доступен в двух лекарственных формах: раствор для приема внутрь и таблетки, покрытые оболочкой. Также есть высококонцентрированная инновационная лекарственная форма таблетки Синупрет® экстракт (BNO 1016), содержащая сухой нативный экстракт с 4-кратной дозировкой активных веществ в разовой дозировке для взрослых по сравнению с Синупрет таблетки. [12, 13].
Препараты произведены по концепции фитониринг (от фито – растительный, инжиниринг – технология).
Фитониринг® — концепция производства растительных препаратов, позволяющая с помощью самых современных научных методов выявлять высокоэффективные действующие вещества растений и на их основе разрабатывать и производить новые лекарственные препараты, используя передовые научные знания в области фармации.
Доказательная база: (обобщенные клинические данные см. табл. 1 Приложения)
· 3 клинических исследования,
· объединенный анализ двух клинических исследований
· нерандомизированное исследование Синупрета при ОРС.
Выводы:
· рандомизированные исследования с большим уровнем достоверности продемонстрировали превосходство Синупрета над плацебо у пациентов с бактериальным или вирусным РС,
· в открытом исследовании, в котором сравнивали Синупрет® с интраназальным спреем флутиказона фуроатом (ФФ), были получены доказательства эффективности и безопасности Синупрета [16].
Экстракт пелларгонии сидовидной (Pelargonium sidoides, EPs 7630)
О препарате:
Корни Pelargonium sidoides в течение длительного времени использовали в традиционной медицине зулусских племен, но современная синтетическая форма в виде жидкого растительного экстракта, также известного как EPs 7630, стала доступна только недавно [18, 19].
EPs 7630 продемонстрировал:
· противовирусный,
· иммуномодулирующий эффект in vitro [20, 21].
Доказательная база (обобщенные клинические данные см. табл. 2 Приложения):
· 2 рандомизированных плацебо-контролируемых исследования использования EPs 7630 при ОРС.
Выводы:
· в совокупности данные имеющихся исследований предполагают, что оптимальной дозой EPs 7630 может являться стандартная доза. Сообщения о нежелательных явлениях (НЯ) чаще поступали при приеме EPs 7630, чем при приеме плацебо;
· при оценке эффективности EPs 7630 для лечения неосложненного ОБРС в исследовании А. Perić и соавт., не выявлено значительных различий между группами в абсолютном улучшении при оценке ринореи и стекании слизи в носоглотке;
· в исследовании А. Perić и соавт. (2020 г.) ни в одной из групп не получено сообщений о НЯ, а анализы культур выявил меньшее количество типов бактерий в образцах из средней части носового хода для группы EPs 7630 по сравнению с группой амоксициллина [25].
Цикламен (Cyclamen europaeum)
О препарате:
Cyclamen europaeum долгое время использовался в Юго-Восточной Европе для лечения болезней носоглотки [26]. Однако первые рандомизированные исследования, оценивающие эффективность и безопасность этого препарата при ОРС, стали доступны совсем недавно [27, 28]. В нынешнем составе водно-спиртовой экстракт цикламена содержит долю сапонинов [28]. При интраназальном введении экстракт вызывает рефлекторное, быстрое, обильное и часто болезненное отделение слизи за счет холинергического эффекта, продолжающегося около 30 мин. [28, 29].
Доказательная база (обобщенные клинические данные см. табл. 3 Приложения):
Выводы:
· Кокрановский метаанализ, опубликованный в 2018 г. на основе двух исследований, показал, что эффективность цикламена неизвестна,
· НЯ, включая раздражение в носу и горле, несильное носовое кровотечение и чихание, были чаще отмечены при использовании назального спрея, чем при применении плацебо (относительный риск – ОР 2,11; 95% ДИ 1,35–3,29) [30],
· авторы также подчеркнули необходимость проведения дальнейших РКИ для оценки эффективности его использования в лечении ОРС [30].
ГелоМиртол® форте
О препарате:
ГелоМиртол® форте представляет собой дистиллят смеси четырех ректифицированных эфирных масел [31]. Доклинические исследования показали, что этот продукт обладает:
· антиоксидантным,
· муколитическим,
· противовоспалительным
· антимикробным действием [32, 33].
Доказательная база (обобщенные клинические данные см. табл. 4 Приложения):
· ГелоМиртол® был впервые испытан в клинических условиях в 1995 г. с участием здоровых добровольцев в ходе исследования, которое продемонстрировало его муколитическое и возбуждающее секрецию действие [34].
· РКИ также продемонстрировали эффективность этого продукта при хроническом и остром бронхите [35, 36]. При поиске литературы обнаружено одно двойное слепое РКИ ГелоМиртола® при ОРС.
Выводы:
· в сравнительном плацебо-контролируемом исследовании с неуказанным эфирным маслом изменения в оценке симптомов по сравнению с исходным уровнем были более значимыми при приеме ГелоМиртола® и эфирного масла, чем при приеме плацебо,
· исследование потенциально ограничено выборочной отчетностью о результатах [7, 37], подчеркивая необходимость в дополнительных данных, описывающих профиль эффективности и переносимости ГелоМиртола®.
Цинеол
О препарате:
Цинеол – основной активный компонент ГелоМиртола® [39], а также основной компонент эвкалиптового масла [40]. Как и другие растительные препараты, цинеол обладает:
· противовоспалительными
· антимикробными свойствами [41].
При проведении испытаний независимо от ГелоМиртола® он показал эффективность при различных респираторных заболеваниях, включая астму, хроническую обструктивную болезнь легких и острый бронхит [42].
Доказательная база (обобщенные клинические данные см. табл. 5 Приложения):
· одно двойное слепое плацебо-контролируемое рандомизированное исследование цинеола при ОРС
Выводы:
· ни один пациент не сообщил о НЯ в группе плацебо, в то время как 5 пациентов группы цинеола сообщили о головной боли, боли в ушах, носовом кровотечении, сведении мышц, изжоге и экзантеме,
· авторы считают, что изжога и экзантема связаны с цинеолом,
· данные об эффективности и безопасности цинеола, полученные в исследованиях, требуют подтверждения в дальнейших крупномасштабных клинических исследованиях.
В рамках изучения доказательной базы среди всех растительных препаратов, которые вошли в настоящий анализ, было обнаружено одно рандомизированное исследование [43] и одно неинтервенционное исследование, сравнивающие растительные препараты между собой [31].
(табл 6, см Приложение)
На основании этих исследований авторы пришли к заключению, что существует необходимость проведения дальнейших рандомизированных сравнительных исследований растительных препаратов для дифференциации и определения свойств каждого из них.
Синтетические препараты
Мометазона фуроат
О препарате:
Назальный спрей на основе МФ используют с 1998 г. для лечения воспалительных заболеваний носа [45].
МФ – глюкокортикостероид, который в некоторых странах, включая и РФ, показан при рините и ОРС [45]. Считается, что при ОРС противовоспалительные свойства МФ опосредуют его положительные эффекты [45].
Доказательная база (обобщенные клинические данные см. табл. 7 Приложения):
· 3 клинических исследования МФ при ОРС,
· один Кокрановский метаанализ,
· 2 предварительных анализа того же исследования.
Выводы:
Оценка отдельных симптомов, таких как заложенность носа, боли в лице, ринорея и стекание слизи в носоглотке или кашель, показала более значимое улучшение при использовании МФ, чем при приеме плацебо:
· большинство НЯ были легкой или умеренной интенсивности, но включали головную боль и носовое кровотечение,
· тест на стимуляцию адренокортикотропного гормона показал отсутствие подавления гипотоламо-гипофизарно-надпочечниковой оси МФ,
· большая эффективность более высокой дозы МФ была подтверждена в Кокрановском метаанализе [51].
N-ацетилцистеин
О препарате:
В настоящее время двумя основными показаниями к применению N-ацетилцистеина являются хроническая обструктивная болезнь легких и передозировка парацетамола [43, 44]. Препарат представляет потенциальный интерес для лечения ОРС благодаря его муколитическому и антиоксидантному действию [52, 53] и влиянию на густоту назальной слизи.
Доказательная база (обобщенные клинические данные см. табл. 8 Приложения):
· 2 клинических исследования N-ацетилцистеина при ОРС
По результатам исследования M. Bahtouee и соавт. пришли к выводу:
· добавление N-ацетилцистеина к традиционному лечению не приносит пользу при остром синусите.
В другом исследовании:
· авторы сообщили о более высокой доле пациентов с улучшением к концу лечения в группе N-ацетилцистеина (82,67%), чем в группе амброксола (50,67%); p<0,0001,
· в месяцы 3 и 6 количество случаев обострения РС после предыдущего эпизода также было ниже в группе N-ацетилцистеина, чем в группе амброксола.
Приложение (посмотреть все таблицы)
оценка


